UČEBNÉ TEXTY
|
1 Lokalizované
a delokalizované p väzby Vo viacerých látkach
je p
väzba presne umiestnená – lokalizovaná
– medzi dvoma susednými atómami, napr.: O = O, H2C =
CH2.
V mnohých látkach však väzba p
ovplyvňuje aj väzby medzi susednými atómami napr.: v nenasýtených
uhľovodíkoch, heterocyklických zlúčeninách, aniónoch CO32-,
SO42-.
Takéto väzby nazývame delokalizované,
čo znamená, že väzbové elektróny p
sa rovnomerne rozprestierajú v poli viacerých jadier viazaných
atómov.
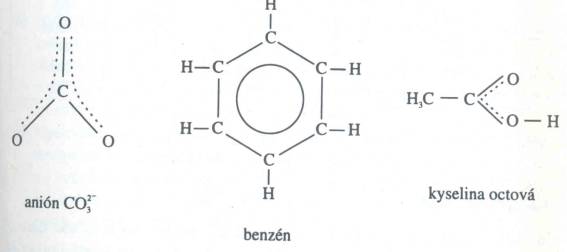
Obr. č. 1: Znázornenie delokalizovaných p
väzieb v molekulách a iónoch Napríklad
dvojité väzby v benzéne sú rovnomerne rozdelené –
delokalizované po celej molekule benzénu. Väzby medzi všetkými
atómami uhlíka v molekule benzénu sú rovnocenné. Pri
delokalizácii sa uvoľní energia a vzniká stabilnejší
systém, ako keby boli väzby lokalizované.
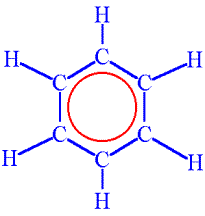
Obr. č. 2: Ukážka rovnomerného rozdelenia dvojitých väzieb v molekule benzénu
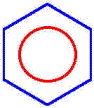
Obr. č. 3: Ukážka vzniku konjugovaného systému
v molekule benzénu
|
Posledná aktualizácia: 04.10.2004