UČEBNÉ TEXTY
|
5.2
Kovová väzba Kovy, ktoré tvoria ¾ prvkov PSP, majú odlišné vlastnosti v porovnaní so
zlúčeninami s kovalentnými alebo iónovými väzbami. Za bežných
podmienok sa kovy (okrem ortuti) vyskytujú v tuhom skupenstve.
Pre kryštálovú štruktúru kovov je charakteristické najtesnejšie
usporiadanie častíc. V kryštáli kovu je jeden atóm
obklopený 8 alebo 12 ďalšími atómami kovu. Fyzikálne
vlastnosti kovov (lesk, tepelná a elektrická vodivosť,
kujnosť...) poukazujú na to, že väzby v kovoch sa líšia
od kovalentných a iónových väzieb.
Obr. č. 33: Ukážka štruktúry kovov a lítia
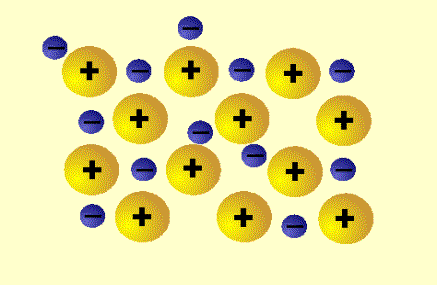
Valenčné elektróny sa z pôvodných atómov uvoľňujú, pohybujú sa medzi vzniknutými katiónmi a sprostredkúvajú ich vzájomnú väzbu. Väzba v kovoch sa nazýva kovová väzba. Väzbu v kryštálovej štruktúre kovu si možno predstaviť ako množstvo pohyblivých elektrónov, ktoré sa nachádzajú okolo kladne nabitých iónov.
Obr. č. 34: Schéma kryštálovej štruktúry kovu
|
Posledná aktualizácia: 04.10.2004